Когда дело доходит до природного газа, вы не должны быть незнакомы с ним, и в настоящее время ни одно домохозяйство не может готовить без него. Основным компонентом природного газа является метатан, который является одним из самых простых углеводородных соединений. Ускорение развития и использования метана является ключом к реализации зеленого и устойчивого развития энергетической и химической промышленности. В дополнение к его прямому использованию в качестве топлива, метан также может использоваться в качестве ресурса C1, то есть молекула, которая содержит атом углерода и может продолжать преобразовать для приготовления химических веществ с высокой стоимостью, таких как метанол, коммерческий кислота и так далее. Метан может быть сожжен в кислороде с образованием воды и углекислого газа. Без сжигания можно ли активировать и преобразовать углеводородные связи молекул метана в легких условиях? Ответ да! Это реакция "Святого Грааля" в области катализа. Реакции, связанные с «святым Граалем», часто чрезвычайно сложны, так как, возможно, потребуется выполнять в очень резких условиях, или им может потребоваться преодолеть неотъемлемые трудности химической реакции, таких как активация высокостабильных соединений, низкие урожайность и низкая селективность. Эти проблемы затрудняют реализацию этих реакций, но если они могут быть успешно достигнуты, они приведут к значительным прорывам в научных исследованиях и промышленном применении.

1. Художники при преобразовании метана при низких температурах Очень трудно преобразовать метатан непосредственно в другие полезные химические вещества с недорогим кислородом при низких температурах или даже в комнатной температуре, почему это так? Давайте посмотрим на природу метана и кислорода. Химическая структура метана содержит четыре идентичных углеродных связей (CH), которые образуют очень симметричную ортотетраэдрическую конфигурацию, и каждая связь CH3-H метана имеет энергию связи до 435 кДж/моль. Мы можем думать о связке метана как о особенно сильной пружине. Эта весна очень натянута и требует большой силы, чтобы растянуть. В химии эта «сила» - это энергия, необходимая для разрыва связи СН. Эта высокая энергия связывания делает связи метана с помощью метана термодинамически стабильной и очень трудно сломать или реагировать с нормальными условиями. С другой стороны, в химических реакциях реактивные группы обычно генерируются при полярном взаимодействии (полярное взаимодействие - это явление о том, что молекула имеет один конец положительно заряженный, а другой заряжен), тогда как симметричная структура и неполярная природа метена предотвращают молекулу. Это из -за создания такой полярности (в соответствии с молекулярной конфигурацией, молекула с плоской симметрией не имеет полярности) и не может обеспечить реактивные группы. Следовательно, активация и преобразование метана очень сложны и обычно требуют жестких условий, таких как высокие температуры (600-1100 ° C) или некоторые «экстремофилы», такие как сверхпрочные кислоты и свободные радикалы, чтобы помочь в активации метана. Следовательно, основная трудность в реализации низкотемпературной активации метана и кислорода заключается в том, как активировать связь СН метана, то есть, как растянуть «пружину» в связи СН. 2. Чудо катализатора Ученые придумали хорошее решение этой проблемы и решили использовать катализатор, чтобы помочь активировать метатан при низких температурах (катализатор - это химическое вещество, которое не изменяется до или после реакции, но ускоряет реакцию, изменяя минимальное количество энергии, которая должна быть введена для реакции, состоящейся). В 2023 году журнал природный катализ сообщил о процессе достижения прямого преобразования метана с кислородом в оксиды C1 (метанол (CH3OH), муравьиная кислота (HCOOH) и метиленгликол (HOCH2OH) с использованием специфического молибденового дисульфида (MOS2) Катализатор при 25 ° C. Преобразование метана 4,2% и почти 100% оксигенатов С1 были достигнуты путем превращения метана и кислорода в ценные оксигенаты С1 в условиях окружающей среды. Этот MOS2 является единственным катализатором, о котором сообщалось до сих пор, который может реализовать преобразование температуры в комнатной температуре метана и кислорода. Все это связано с уникальной геометрией и электронной структурой сайта МО на краю MOS2. Этот сайт MO обладает высокой активностью активации в направлении кислорода в водной среде, образуя волшебный O = Mo = O* виды. Этот вид облегчает нарушение углеродной связи и снижает энергию активации связи метана, тем самым значительно увеличивая реакционную способность метана и, таким образом, реализуя низкотемпературную активацию метана и кислорода. Это открытие принесет больше возможностей для будущего использования энергии и защиты окружающей среды, а также даст нам более глубокое понимание удивительной роли катализаторов и вспомогательных организаций.
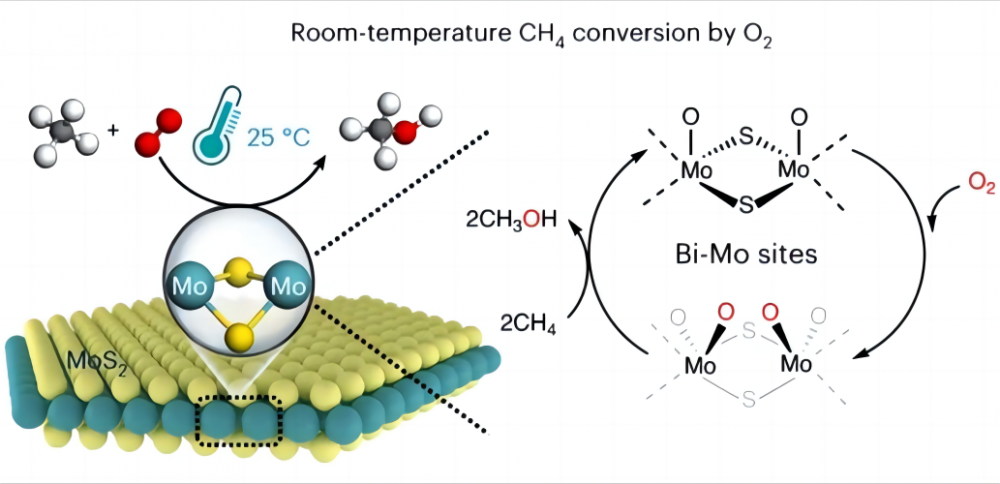
3. Познаваемая стратегическая значимость низкотемпературной активации метана Реализуя прямое каталитическое превращение метана и кислорода при комнатной температуре и превращение метана в природное газ в другие полезные химические вещества, может значительно улучшить частоту использования природного газа, уменьшить отходы и лучше защитить окружающую среду и реализовать устойчивое развитие энергии Полем Во -вторых, в качестве парникового газа, метана уступает только углекислым газам в его вкладе в глобальное потепление. Если метан может быть преобразован в другие вещества, он может помочь нам уменьшить излучение загрязнителей воздуха (например, оксиды углерода, оксиды азота, оксиды серы, углеводороды и эфирные соединения) и ослабить давление глобального потепления.




